11月CDE生物制品药审报告
导读:21个新药品种获批上市
看点
•11月药审中心受理总量为1510个
•11月21个新药品种获批上市
•11月新增100个按仿制药质量和疗效一致性评价申报的受理号
•用于糖尿病足溃疡,由两岸合作共同研发的香雷糖足膏上市
根据药智数据企业版——药品注册与受理数据库最新统计,2023年11月份CDE共承办新的药品注册申请以受理号计有1510个,其中化药受理1034个,中药受理290个,生物制品受理186个;2023年7-11月各类药品注册申请受理情况详见图1。
PS:药智网公众号【ID:yaozh008】后台回复【11月CDE药审】,即可获取本文表格excel格式文档图片图片图片
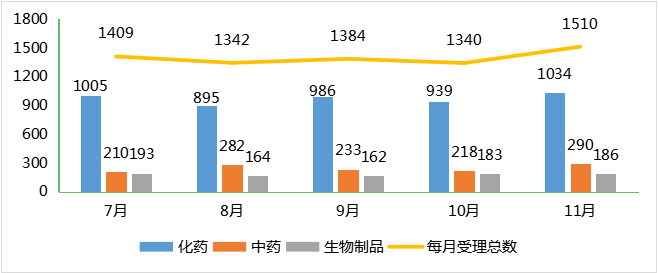
图1 2023年7-11月CDE药品受理情况
2023年11月份(注:状态开始时间(药智)从2023年11月1日至2023年11月30日)完成审评的受理号共1447个,其中化药完成审评976个,中药审评完成289个,生物制品完成审评182个;2023年7-11月各类药品完成审评情况详见图2。(注:完成审评的数据统计截至2023年12月06日)。
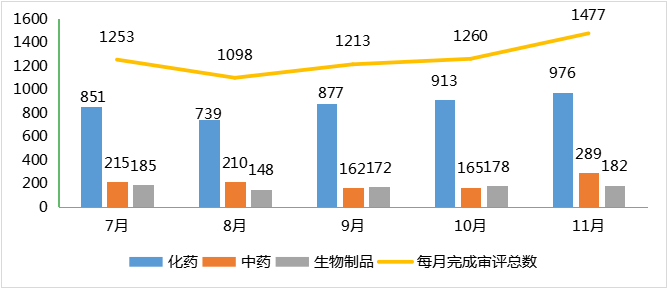
图2 2023年7-11月CDE药品完成审评情况
03
生物制品审评情况
(一)生物制品受理情况
11月份CDE承办新的生物制品注册申请受理号共计186个,新药83个,补充申请62个,进口27个,进口再注册2个;2023年7-11月CDE生物制品各申请类型受理情况详见图8。
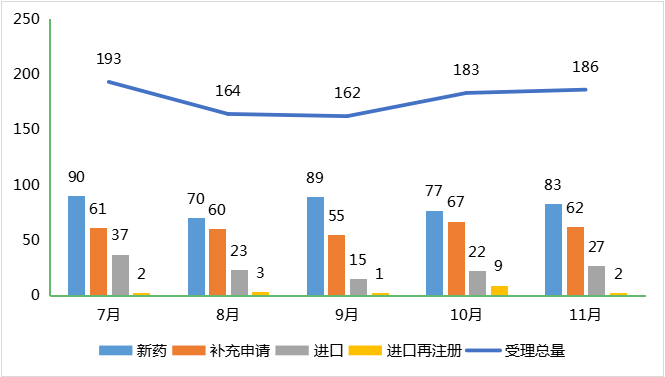
图8 2023年7-11月CDE生物制品各申请类型受理情况
1.生物制品1类新药申报情况
11月共84个生物制品1类新药受理号获得承办,其中,临床试验申请83个,上市申请1个,目前均已进入相应序列排队待审;下表为11月新承办的生物制品1类创新药。
表7 2023年11月新承办的生物制品1类新药

注:排队序号截至2023年12月06日
(二)生物制品完成审评情况
11月份CDE完成审评的生物制品注册申请182个(以受理号计),其中新药申请受理号86个,进口受理号22个,补充申请61个;以审评任务类别统计(以受理号计),临床试验申请88个,上市申请20个;2023年11月CDE生物制品各审评任务类别完成审评情况详见图9。(注:完成审评的数据统计截至2023年12月06日)。
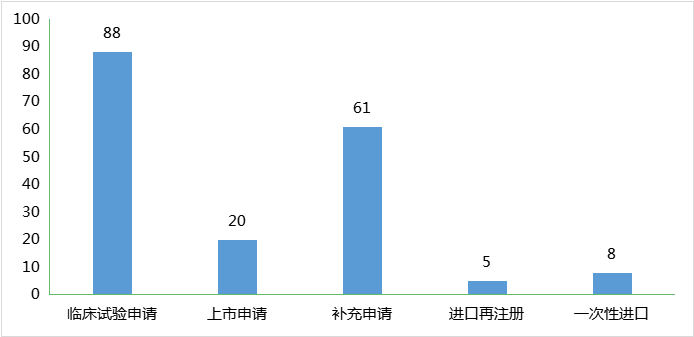
图9 2023年11月CDE生物制品各审评任务类别完成审评情况
在受理号审评结论方面:批准临床94个,批准生产5个,批准进口5个,未被批准6个;下表为11月生物制品批准上市信息。
表8 2023年10月生物制品获批信息
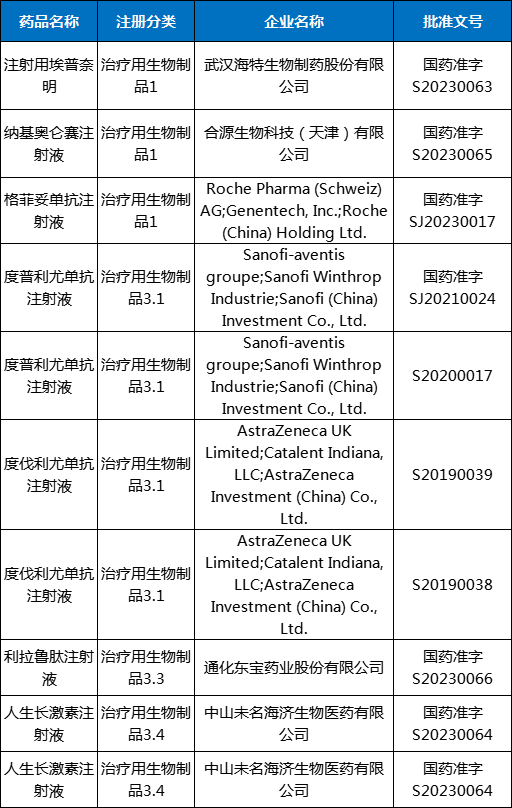
数据来源:药智数据企业版——药品注册与受理数据库、药智数据企业版——仿制药一致性评价分析系统数据库

用户登录
还没有账号?
立即注册