武汉病毒所张波团队在西尼罗病毒新型减毒疫苗的设计方面取得新进展
2021-08-17
2021年08月06日,国际学术期刊“EMBO Molecular Medicine”在线发表了中国科学院武汉病毒研究所/生物安全大科学研究中心张波团队与北京舜雷科技有限公司的联合研究成果。论文题为“Rational design of West Nile virus vaccine through large replacement of 3? UTR with internal poly(A)”(http://doi.org/10.15252/emmm.202114108)。该研究通过理性化设计,以多聚腺苷酸poly(A)序列替换西尼罗病毒3?非编码区(3? UTR)的毒力基因序列,构建了西尼罗病毒新型减毒活疫苗。西尼罗病毒(WNV)属于黄病毒家族,由于黄病毒基因组3? UTR二级结构的相似性,该方法有望成为高致病黄病毒减毒活疫苗理性化设计的通用新策略。
黄病毒是在全球广泛分布的一类重要的虫媒病毒,除WNV外,还包括登革病毒(DENV)、寨卡病毒(ZIKV)、日本脑炎病毒(JEV)、黄热病毒(YFV)、蜱传脑炎病毒(TBEV)和鄂木斯克出血热病毒(OHFV)等。黄病毒感染可引起出血热、脑炎等神经系统损伤,更严重的可导致死亡,严重危害人类的生命健康,是新发传染性疾病的重要来源,已成为全球面临的重要公共卫生问题之一。目前针对黄病毒感染尚无有效的抗病毒药物和治疗方法,用于人类预防的黄病毒疫苗也仅有4种,因此开发更为有效的新型黄病毒疫苗对我国乃至世界范围内黄病毒的防治均具有重要意义。在众多的疫苗类型中,减毒活疫苗因其免疫原性强,单次免疫即可引起较高水平的体液和细胞免疫应答,诱导全面而持久的免疫保护的特点,在疫苗研发中日益受到重视。
黄病毒基因组3? UTR作为一个重要的功能元件,在病毒的毒力、复制、传播和种属特异性等方面发挥重要的作用。3? UTR约400-700 nt,可形成系列的RNA二级结构,含有SL、DB和sHP-3’SL三个区域。其中SL和DB作为基因组复制非必需原件,在调节病毒毒力、宿主免疫反应以及跨种传播等方面发挥了重要的作用,是重要的减毒活疫苗设计靶点。
本研究以WNV为模型,利用分子生物学手段,以poly(A)序列替换3? UTR的SL和DB区域,构建了含有不同长度poly(A)的感染性克隆文库,并通过进化筛选的方法成功获得含有poly(A)(约130 nt)替换序列的重组病毒WNV-poly(A)。基本病毒学特征分析结果表明WNV-poly(A)能够在Vero细胞上高效增殖,滴度高达107 PFU/ml;小鼠毒力实验表明WNV-poly(A)神经侵袭力显著降低,毒力相对于野生型(WT)病毒降低了1万倍以上;WNV-poly(A)单次免疫即可诱导小鼠产生较高水平的体液和细胞免疫反应,且104 PFU低剂量免疫就可以为小鼠提供完全的高剂量(3×107 PFU,WT WNV)攻毒保护,并能提供长期的完全免疫保护。进一步研究发现,WNV-poly(A)与WT相比对I型干扰素更敏感,这可能是导致其减毒的原因之一。另外,将WNV-poly(A)病毒在Vero细胞上连续传代50代后,发现其poly(A)序列保持稳定,毒力以及免疫保护效果与传代前无显著差异,说明了WNV-poly(A)作为减毒疫苗具有良好的遗传稳定性和安全性。
武汉病毒所博士生张亚南,博士生李娜以及博士后张秋艳为论文共同第一作者,武汉病毒所张波研究员为通讯作者。该研究得到了北京舜雷科技有限公司的资助。
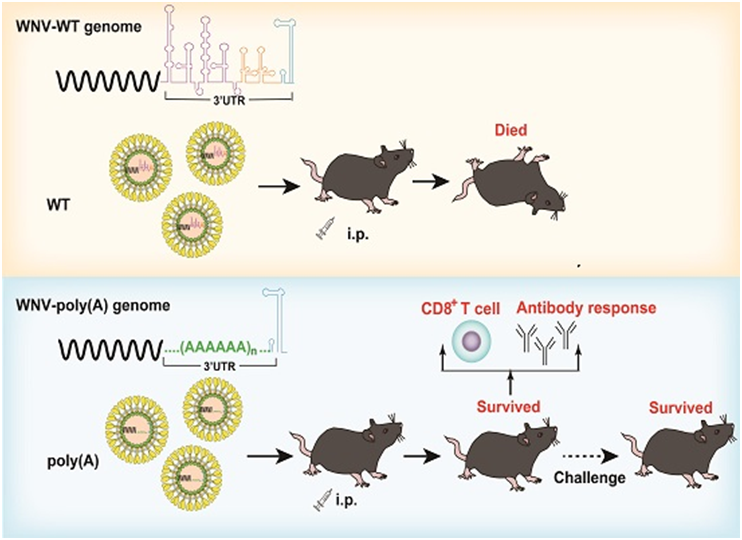
图1.WNV-poly(A)减毒活疫苗的构建及应用
原文出处:Zhang YN, Li N, Zhang QY, Liu J, Zhan SL, Gao L, Zeng XY, Yu F, Zhang HQ, Li XD, Deng CL, Shi PY, Yuan ZM, Yuan SP, Ye HQ, Zhang B. Rational design of West Nile virus vaccine through large replacement of 3' UTR with internal poly(A). EMBO Mol Med. 2021 Aug 5:e14108. doi: 10.15252/emmm.202114108. Epub ahead of print. PMID: 34351689.
链接:https://pubmed.ncbi.nlm.nih.gov/34351689/

用户登录
还没有账号?
立即注册