-
2021-12-10
2021-12-10 12月2日,国务院联防联控机制科研攻关组疫苗研发专班工作组组长郑忠伟表示,我国正在快速推进奥密克戎株疫苗研发。 12月1日,美国疾病控制与预防中心宣布,在加州确认了该国首例奥密克戎变异毒株感染病例,受此消息影响,美股盘中大幅跳水,走势彻底逆转。 同日,世卫组织表示,目前已在27个国家和地区发现奥密克戎毒株,大部分病例与旅行相关。此外,初步证据表明,与其他需要关注的变异株相比,奥密克戎再感染风险可能更高。 但由于奥密克戎出现的时间较短,样本量较小,WHO对于其传播能力和严重程度仍无法定性。在过去六十天搜集的830110份病毒基因序列样本中,99.8%的样本为德尔塔毒株,奥密查看更多 -
2021-12-06
2021-12-06 近日,默沙东(MSD)公司宣布,美国FDA已授予15价肺炎球菌结合疫苗Vaxneuvance的补充生物制品许可申请(sBLA)优先审评资格,用于帮助6周至17岁儿童预防侵袭性肺炎球菌导致的疾病。 肺炎球菌疾病是由肺炎链球菌感染引起的疾病,对儿童的影响与成人不同,2岁以下儿童特别容易感染肺炎球菌。某些肺炎球菌血清型对儿童危害更大,包括血清型22F、33F和3,它们占5岁以下儿童所有侵袭性肺炎球菌疾病病例的四分之一以上。 Vaxneuvance是一款15价肺炎球菌结合疫苗,由与CRM197载体蛋白结合的肺炎链球菌血清型1、3、4、5、6A、6B、7F、9V、14、18C、19查看更多 -
2021-12-06
2021-12-06 导读:包括单药治疗和联合用药。 12月4日,北京神州细胞宣布控股子公司神州细胞工程收到国家药品监督管理局核准签发的《药物临床试验批件》,公司在研产品SCTA01C 注射液以及 SCTA01C 注射液与 SCTA01 注射液联合使用的临床试验申请获得批准(批件号:2021L90025、2021L90026、2021L90027)。 其中批件 2021L90025 为 SCTA01C 单药临床研究方案,批件 2021L90026、2021L90027 为 SCTA01C 与 SCTA01 组合用药临床研究方案。 SCTA01 是神州细胞工程自主开发的重组抗 SARS-CoV-查看更多 -
2021-12-03
2021-12-03 12月1日,赛诺菲宣布,已与奥地利私营生物技术公司Origimm biotechnology GmbH达成收购协议,此次收购预计将于2021年12月初完成,交易尚未披露价格及具体细节条款。 公开信息显示,Origimm是一家生物技术研发公司,致力于从引起皮肤疾病的细菌(如痤疮)中发现有毒的皮肤微生物组成分和抗原。此次交易将使ORI-001整合到赛诺菲的早期研发管线。ORI-001是一种基于重组蛋白的治疗性寻常痤疮候选疫苗,该疫苗已于2021年第三季度进入初步临床研究。 通过此次收购,赛诺菲将继续执行其全球Play to Win战略,寻求增长机会并建立行业领先的疫苗管线。据查看更多 -
2021-12-01
2021-12-01 日前,挪威临床阶段生物制药公司Nykode Therapeutics宣布与再生元(Regeneron)达成了高达9亿美元的癌症和传染病DNA疫苗合作交易。 这笔交易包括3000万美元的预付款和2000万美元的股权投资,再加上基于未来潜在开发和商业成就的额外付款,最高可达到8.75亿美元和版税,而再生元将承担研究以及潜在临床、监管、生产和商业化活动的费用。 此次与再生元的合作涵盖了5个项目多个适应症目标,其中两项重点针对传染病疫苗,三项针对癌症,每一种候选疫苗都有资格获得里程碑和专利权使用费。Nykode将负责疫苗的生产和设计,以及1期临床试验结束前的产品供应。再生元将负责查看更多 -
2021-12-01
2021-12-01 导读:预计针对新冠病毒奥密克戎变异株的新型疫苗可在100天内进入临床试验阶段。 12月1日,云顶新耀与Providence Therapeutics(以下简称“Providence”)共同宣布,已开始开发专门针对新冠病毒奥密克戎(Omicron)变异株的COVID-19疫苗。 两家公司的科学家已对新冠病毒奥密克戎变异株的序列进行了分析,获得了病毒序列,并设计了质粒克隆(plasmid clone)。我们预计针对新冠病毒奥密克戎变异株的新型疫苗可在100天内进入临床试验阶段。查看更多 -
2021-11-30
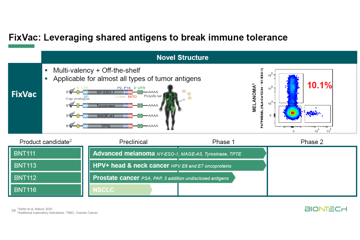
2021-11-30 2021年11月19日,BioNTech公司宣布,美国FDA已授予BNT111快速通道资格。BNT111是一款治疗性mRNA癌症疫苗。它能够编码4种在90%以上黑色素瘤患者中出现的肿瘤相关抗原,通过与PD-1抑制剂联用,防止T细胞耗竭,提高晚期黑色素瘤患者的预后。该候选疫苗目前正在进行一项2期临床试验,在PD-1抑制剂难治/复发性且不可切除的III期或IV期黑色素瘤患者中,评估它的疗效和安全性。 BioNTech的FixVac技术平台利用mRNA表达共享的肿瘤相关抗原,它们可以靶向抗原呈递细胞,激活抗原特异性T细胞反应。该平台的一个优势在于可以提前生成疫苗并保存起来,可以查看更多 -
2021-11-30
2021-11-30 近日,Moderna公司宣布,候选疫苗mRNA-1345的2/3期临床试验已完成首例患者给药,用于预防呼吸道合胞病毒(RSV)感染。RSV是在老年人和幼儿中导致呼吸道疾病的主因之一,目前尚无获批疫苗。在此前的1期临床试验中,受试者接种单剂疫苗后1个月,针对RSV-A的中和抗体几何平均滴度与基线相比提高至少20倍。 RSV是一种常见的呼吸道病毒,一般会引起感冒样症状,RSV感染主要发生在秋季、冬季和春季。这种病毒是导致5岁以下的幼儿和65岁以上的老年人感染严重呼吸道疾病的主因之一,并且可能进展为肺炎等严重疾病。 mRNA-1345是一款编码病毒稳定融合前F糖蛋白的mRNA疫查看更多 -
2021-11-30
2021-11-30 11月24日,中国临床试验注册中心网站显示,沃森生物登记了一项评价新型冠状病毒mRNA疫苗(ARCoVaX )在18~59岁和60岁及以上已接种新型冠状病毒灭活疫苗人群中加强接种免疫原性和安全性的IIIb期临床试验(注册号:ChiCTR2100053551 )。ARCoVaX也是中国首个进入III期临床的国产mRNA疫苗。 ARCoVaX是由艾博生物、沃森生物和军科院军事医学研究院共同研发的一款mRNA疫苗,用于预防由SARS-CoV-2 感染所致的新冠肺炎。它由脂质纳米粒(LNPs) 包裹,靶向SARS-CoV-2棘突蛋白RBD区域。100μg剂量可诱导高水平中和抗体,查看更多 -
2021-11-30
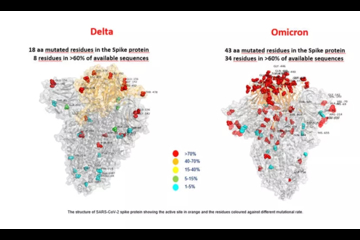
2021-11-30 近日,被世界卫生组织(WHO)命名为Omicron(B.1.1.529)的新冠病毒变种受到广泛关注。因为它在刺突蛋白上携带30多个突变,可能让它具有更强的传播力,并且逃避已有新冠疫苗提供的免疫力。针对这一变种,疫苗开发公司也在积极做出应对。日前,Moderna公司发布声明,介绍了该公司针对Omicron的开发策略。 自从2021年初,Moderna就在针对可能出现的新变种推进综合性研发策略,如果该公司目前的增强疫苗(剂量为50 μg)不足以提高针对Omicron变种的免疫力的话,该公司将在三个层面进行开发。 首先,Moderna已经在健康志愿者中检验了更高剂量增强疫苗(剂查看更多



用户登录
还没有账号?
立即注册